Einleitung
Bei Typ I Diabetes handelt es sich um eine Autoimmun-Krankheit, bei der unter anderem Insulin-produzierende ß-Zellen im Pankreas, zerstört werden und es zu einer α-Zelldysfunktion kommt, die zu einer verminderten Glukagonausschüttung bei Hypoglykämie führt.1,2
Ein Mangel an Insulin führt zu einer Erhöhung des Blutzuckerspiegels. Dieser wird ausserdem durch den Insulin-Antagonisten Glucagon und weitere Gegenspieler des Insulins wie z. B. Cortisol, Adrenalin und das Wachstumshormon, beeinflusst.3 Eine Erhöhung des Blutzuckerspiegels wird auch durch Stress, gewisse immunologische Prozesse, die Zufuhr von Kohlenhydraten und die Gluconeogenese begünstigt. Übergewicht spielt häufig eine wichtige Rolle bei der Entwicklung einer ungenügenden Insulinwirkung.4 Die Insulin Sensitivität ist zirkadian und unterscheidet sich im Tagesverlauf.5 Bewegung und die Ausschüttung von Insulin senken den Blutzuckergehalt.6 Insgesamt bilden die verschiedenen Faktoren ein komplexes System, das der Erhaltung der Glukosehomöostase dient. Betroffene von Typ I Diabetes lernen viele dieser Faktoren zu beeinflussen, wobei die externe subkutane Insulinapplikation und die Selbstkontrolle der Blutzuckerwerte die wichtigsten Hilfsmittel sind. Da Insulin das Potential hat, akute, schwere Hypoglykämien zu verursachen und aufgrund von kardiovaskulären Komplikationen durch erhöhte Blutzuckerwerte sollte versucht werden eine «nahe Normoglykämie» zu erreichen, jedeoch bleibt Typ I Diabetes schwierig zu therapieren und ist mit einem dauerhaften Balanceakt verbunden.7–10
Anamnese, Komorbiditäten und Vorbehandlungen
Die 51-jährige Patientin wurde bereits in Ihrem 5. Lebensjahr mit Diabetes mellitus Typ 1 diagnostiziert und wird seit 25 Jahren in unserer Diabetes- und Hausarztgruppenpraxis betreut. Bei der Patientin besteht ein erhöhtes kardiovaskuläres Risiko durch eine arterielle Hypertonie und Dyslipidämie. Aufgrund einer langandauernden mangelhaften Einstellung des Blutzuckers (BZ) über mehrere Jahre entwickelte sie ausserdem schwerste diabetische Komplikationen. Es besteht eine Makroangiopathie, assoziiert mit einer koronaren Herzkrankheit sowie einer peripheren arteriellen Verschlusskrankheit, welche beide mehrerer Interventionen mit Hilfe von Herzkathetern bedurften. Aufgrund der vorliegenden Mikroangiopathie entwickelte sich eine nach mehreren Lasertherapien beständige proliferative Retinopathie. Ausserdem entwickelte sich eine Makulopathie, eine Neuropathie mit Gastroparese, eine Orthostase, eine Obstipation, eine periphere Polyneuropathie und eine beidseitige Charcot Neuro-Osteoarthropathie, sowie ein chronisches Malum perforans rechts mit Osteomyelitis des Calcaneus. Letzteres führte trotz vorgehender Versorgung durch orthopädische Schuhtechnik schliesslich zu einer Amputation des Unterschenkels. In den letzten Jahren entwickelte sich zunehmend eine chronische Niereninsuffizienz mit nephrotischem Syndrom.
Bei der Erstanamnese vor 25 Jahren, lagen die durchschnittlichen Blutzuckerwerte bei 12 mmol/L (HbA1c ca. 8,5 %) und es zeigten sich starke BZ-Schwankungen. Während der ersten Krankheitsjahre wurde meist ein HbA1c-Wert > 9 % gemessen. Die Patientin litt schon damals unter einer Hypoglykämieangst, hervorgerufen durch mehrere vorausgehende nächtliche Hypoglykämien kurz nach der Diagnosestellung. Im weiteren Verlauf manifestierten sich zusätzlich postprandiale Hypoglykämien bei Neuropathie-bedingter Magenparese. Angesichts der eindeutigen klinischen Hinweise wurde eine Gastroskopie durchgeführt, welche die zurückgebliebene Nahrung zeigte. Auf einen szintigraphischen Nachweis wurde verzichtet. Um eine bessere Einstellung des BZ zu erreichen, riskierte die Patientin tagsüber seit Jahren knapp an der Hypoglykämiegrenze liegende BZ-Werte. Dies führte zu häufigen Hyperglykämien am Tag, die in einer Wahrnehmungsstörung mit verzögerter adrenerger Gegenregulation (ab BZ-Werten < 3 mmol/L) resultierte, was die Problematik verschärfte. Aus der verzögerten adrenergen Gegenregulation gingen schwere Hypoglykämien hervor, teilweise bis hin zur Bewusstlosigkeit.
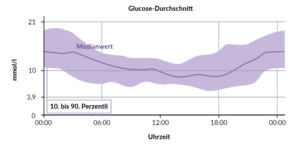
Zur besseren Kontrolle des Blutzuckers wurden der Patientin bereits zu Beginn der Behandlung eine langfristige psychiatrische Begleitung für die Patientin selbst und ihre Kinder, eine regelmässige Diabetes- und Ernährungsfachberatung, sowie eine Gruppenschulung mit funktioneller Insulintherapie (FIT, flexible Anpassung der Insulindosis in Abhängigkeit der Kohlenhydratmenge und des aktuellen BZ-Wertes). Es folgten Hypoglykämie-Awareness Trainings, eine Insulinpumpentherapie und Schulungen zu Verhaltensmassnahmen bei Gastroparese. Ausserdem wurde die Anwendung von Prokinetika empfohlen und eine Ernährungsumstellung zu kleinen, aber häufigeren kohlenhydratarmen Mahlzeiten unter Vermeidung von Kohlenhydraten mit hohem glykämischen Index sowie postprandiale Insulininjektionen unter Inkaufnahme höherer Blutzuckerwerte unmittelbar nach dem Essen. Das Tagesprofil der Blutzuckerkurve der Patientin ist über den gesamten beobachteten Zeitraum durch eine Badewannen-Form gekennzeichnet.
Abbildung 1 zeigt die früheren Werte mit einem HbA1c von 8,3 %, diese Kurvenform persistiert trotz eines aktuell verbesserten HbA1c-Wertes.
Die BZ-Einstellung blieb trotz der ergriffenen Massnahmen weiterhin schwierig, und wird durch starke Schwankungen geprägt im Sinne eines «Brittle Diabetes». Aufgrund dessen, wurde 2012 eine isolierte Pankreastransplantation durchgeführt. Zu diesem Zeitpunkt lag noch keine Niereninsuffizienz vor und die Patientin zeigte daraufhin für einige Jahre einen stabilen Blutzuckerspiegel ohne erforderliche Insulingabe. Die Entwicklung einer chronischen Abstossungsreaktion resultierte jedoch in erneutem Insulinbedarf. Die Immunsuppression wurde sistiert und die Insulintherapie wieder aufgenommen. Derzeit ist die Wiederaufnahme der Insulinpumpe mit einem kontinuierlichen Glucose-Monitoring System (CGMS) durch ein «Semi-/Hybrid-Closed Loop» System geplant.
Aktuelle Befunde
a) Vitalparameter: Body Mass Index (BMI) 21 kg/m2, Blutdruck (BD) 135/80 mmHg.
b) Laborwerte: HbA1c 7,5 %, Kreatinin-Clearance 30 ml/min (Kidney Diseases: Improving Global Outcomes [KIDGO] G3bA3), Kalium/Natrium normwertig, Hämoglobin (Hb) 10,5 g/dl, normochrom, normozytär. Low Densitly Lipoprotein (LDL) Cholesterin 1,4 mmol/L. Proteinuria 2,5 g/24h.
c) BZ-Werte (Messung mittels kontinuierlicher subkutaner Glukosemessung mit Freestyle Libre 2® mit Alarmgrenzen für BZ von < 4,4 mmol/L und > 15 mmol/L): Mittelwert BZ: 10,1 mmol/L (Ziel 8,5 mmol/L), time in range (TIR) 54 % (Ziel > 70 %), time above range (TAR) 29 % (Ziel < 25 %), time below range (TBR) 1 % (Ziel < 4 %), prozentuale Glukosevariabilität 40 % (Ziel < 36 %).
d) Therapie: NovoRapid® (4E) 3x/Tag präprandial und als Korrekturinsulin (nach spezifischen Algorithmen der funktionellen Insulintherapie [FIT]) und Toujeo® (6E) als Basalinsulin. 60 % durchschnittlicher Anteil Basalinsulin zu total injiziertem Insulin pro Tag.11,12 Täglich peroral Angiotensin Converting Enzyme (ACE)-Hemmer, Sodium-Glucose Linked Transporter 2 (SGLT2)-Hemmer, Aspirin cardio und subkutan Erythropoietin 2x/Woche, Proproteinkonvertase Subtilisin/Kexin Typ 9 (PCSK-9)-Hemmer alle 2 Wochen.
Diskussion
Die Patientin profitierte seit der Pankreasabstossung von einer kontinuierlichen subkutanen Blutzuckermessung mit programmierbaren Alarmgrenzen, die einen präventiven Alarm bei abfallenden oder ansteigenden BZ-Werten auslösen.13
Die persistierende nächtliche Hypoglykämieangst und die neuropathisch bedingte Magenparese blieben weiterhin eine sehr grosse Herausforderung und gingen mit hohen BZ-Werten nachts und gehäuft postprandialen Hypoglykämien einher. Hypoglykämien führen mehrere Stunden später zu hohen BZ-Werten durch eine oft überschiessende Kohlenhydratzufuhr und der über Stunden andauernden Gegenreaktion der Insulin-Antagonisten (Adrenalin, Cortisol, Glukagon, Wachstumshormon). Diese Gegenregulation ist bei längerem Verlauf bei Typ 1 Diabetes gestört, wodurch häufig der Anstieg von Adrenalin und Glukagon in der Hypoglykämie ausbleibt. Hypoglykämien sind eine nicht unbedeutende Ursache für die Entwicklung von Langzeit-Komplikationen bei Typ 1 Diabetes Patientinnen und Patienten, vor allem durch exzessives Zuführen von Kohlenhydraten nach Hypoglykämien.14 Bei der Patientin führte dies gelegentlich zu der paradoxen Situation, dass sich das HbA1c trotz Reduzieren des Insulins teilweise sogar verbesserte.
Die sogenannte «Badewannen»-Kurve beschreibt ein Blutzuckertagesprofil, bei dem der Blutzuckerspiegel nach dem Nachtessen ansteigt und erst morgens nach dem Aufstehen wieder in den Zielbereich absinkt.15 Die Hauptursache für einen solchen Verlauf ist die nur sehr schwer therapierbare nächtliche Hypoglykämieangst der Patientinnen und Patienten. Der Blutzucker wird nach dem Nachtessen absichtlich oberhalb des Zielbereichs gehalten, indem entweder weniger prandiales Insulin als notwendig appliziert wird oder indem vor dem Schlafen noch eine Kleinigkeit gegessen wird. Das Ziel hierbei ist es, eine nächtliche Hypoglykämie, der man während des Schlafens schutzlos ausgesetzt ist, zu vermeiden. Die Hypoglykämieangst kommt bei Typ 1 Diabetes häufig vor und spielt eine wichtige Rolle bei Patientinnen und Patienten, deren Blutzuckerspiegel nicht zufriedenstellend einstellbar ist.16 Um diesem Problem habhaft zu werden, sollte vor allem in den ersten Jahren nach der Diagnose, bis genügend Erfahrung im alltäglichen Umgang mit Insulin besteht, ein besonderes Augenmerk auf die Vermeidung schwerer Hypoglykämien gelegt werden. Um diese Situation zu vermeiden, halten Diabetologen die Zielblutzuckerwerte in der Anfangszeit der Insulintherapie generell etwas höher Besteht erst einmal eine Hypoglykämieangst, ist diese sehr schwierig zu therapieren und die Patientinnen und Patienten werden meist lebenslang davon begleitet. Dies ist besonders bedenklich, da die Nacht etwa 1/3 der Lebenszeit ausmacht und damit zu einem Grossteil zur Entwicklung von Komplikationen beiträgt.
Im geschilderten Fall kam es aufgrund der lange unzureichenden Blutzuckereinstellung mit entsprechend hohen HbA1c-Werten zu einer neuropathischen Magenparese. Diese unterstützt zusätzlich die Badewannen-Form des Blutzuckertagesprofils, da die Nahrung und somit auch die aufgenommenen Kohlenhydrate länger im Magen bleiben und erst abends aus dem Magen in den Darm zur Resorption weitergeleitet werden. Bei der Patientin führte dies zu einem verzögerten Ansteigen des BZs, oft erst viele Stunden postprandial. Entsprechend führte die Magenparese zu früh-postprandial auftretenden Hypoglykämien durch rasch nach dem Essen wirkendes Insulin. Dies akzentuiert die Hypoglykämieproblematik tagsüber und wird noch verstärkt durch den Versuch die nachts absichtlich höher gehaltenen BZ-Werte, tagsüber aktiv durch Werte nahe an der Hypoglykämiegrenze auszugleichen.
Differentialdiagnostisch muss bei Veränderungen des Insulinbedarfs und damit zusätzlichen BZ-Schwankungen auch eine Dysthyreose (generell leicht höhere BZ-Werte), eine Nebenniereninsuffizienz (weniger Insulinbedarf, mit Hypoglykämien vor allem nachts) oder eine Sprue (Resorptionsstörungen von Kohlenhydraten) in Betracht gezogen werden. Alle diese Störungen treten im Rahmen eines polyglandulären Autoimmunsyndroms mit einer Lebensprävalenz von ca. 15–30 %, gehäuft bei Diabetes Mellitus Typ 1 auf.17 Diese Krankheiten wurden daher im Laufe der Betreuungsjahre bei der Patientin immer wieder ausgeschlossen.
Der Blutzuckerverlauf der Patientin ist in Abbildung 2 dargestellt. Die Dosis an Basisinsulin sollte vor allem anhand der Verstoffwechselung der Glucose, welche nachts vor allem aus der Produktion der Leber stammt, bestimmt werden. Schnell wirkendes Insulin hingegen, sollte vorwiegend an die Menge der tagsüber oral zugeführten Kohlenhydrate angepasst werden. Da in der Nacht meistens keine Nahrung zugeführt wird, bedeutet ein identischer BZ zur «Bedtime» (=unmittelbar vor dem Schlafen gemessener Blutzucker) und morgens beim Aufstehen, dass das basale Insulin nachts richtig dosiert wurde, unabhängig davon, ob beide Werte hoch oder normal sind. Dies spiegelt sich auch in einer Badewannen-Kurve wider. Der Vergleich «Bedtime»-BZ versus BZ morgens ist deshalb ein zentraler Punkt in jeder Beurteilung von BZ-Profilen.
Ein fast physiologisches Verhältnis von Basisinsulin zu Gesamtinsulin von 30–50 % ist ebenfalls ein Hinweis für eine optimale Dosierung des Basalinsulins. Oft wird die tägliche Kohlenhydratzufuhr durch Patientinnen und Patienten mit Typ 1 Diabetes selbst eingeschränkt, um die Dosis an schnell wirkendem Insulin reduzieren zu können; damit wird der prozentuale Anteil an Basalinsulin erhöht (60 % bei der beschriebenen Patientin). Manchmal ist es schwierig abzuschätzen, welches der richtige Basalratenanteil des Insulins ist, da rasch wirkendes Korrekturinsulin (als Basalratenersatz) bei höheren BZ-Werten unabhängig der Mahlzeiten angewendet wird. Ein sogenannter «Mahlzeiten-Auslass-Test kann helfen: Ist der Blutzucker während des Tests stabil, so kann man davon ausgehen, dass die Basalrate richtig eingestellt ist. Bei der beschriebenen Patientin, die solche Tests regelmässig durchführte, war die Basalrate meist korrekt eingestellt.
Wenn der «Bedtime»-BZ im Zielbereich, der BZ morgens aber erhöht ist, sind 3 klassische Differentialdiagnosen (Abbildung 3) zu erwägen. Diese Differentialdiagnosen können durch Analyse der nächtlichen BZ-Messung unterschieden werden:
-
Überschiessende Kohlenhydratzufuhr nach Hypoglykämie nachts. Der früher in der Literatur beschriebene Smogyi Effekt, der eine Gegenreaktion mit hohen BZ-Werten frühmorgens nach einer Hypoglykämie nachts beschreibt, kann zu einem vergleichbaren Profil führen. Jedoch wird dieser Effekt wissenschaftlich heute als fraglich bis inexistent beurteilt und aufgrund der gestörten adrenergen Gegenregulation bei langjährigem Typ 1 Diabetes als sehr unwahrscheinlich eingestuft. Häufig ist hingegen der Grund der überschiessende Kohlenhydratzufuhr.18
-
Zu wenig basales Insulin, um die hepatische Glukoseabgabe nachts abzudecken: kontinuierlicher BZ-Anstieg von der «Bedtime»-Messung bis zum frühen Morgen hin; morgens dann regelmässig zu hoher BZ, wenn das Depot der Leber tagsüber mit genügend Kohlenhydraten oral gefüllt wurde.
-
Dawn- oder Sonnenaufgangsphänomen:19 BZ gegen 03 Uhr ist identisch zum «Bedtime»-BZ; Ansteigen der BZ-Werte zum Morgen hin erst danach; kann durch die zirkadiane Rhythmik der endogenen Insulinantagonisten (z. B. Adrenalin, Wachstumshormon, Glukagon und Cortisol) erklärt werden.
Die Patientin hatte im Laufe Ihrer Diabeteserkrankung trotz der Hypoglykämieangst immer wieder absichtlich zu wenig basales Insulin eingesetzt, obwohl der BZ im «Bedtime»-Zielbereich lag. Ein ausgeprägtes Dawnphänomen, das auch durch angeborene Ausprägung des Biorhythmus vorkommen kann, lag nicht vor.
Weitere Gründe, welche im Laufe der Diabeteserkrankung der Patientin zu vermehrten BZ-Schwankungen und Akzentuierung der Gefahr von nächtlichen Hypoglykämien führten, waren:
-
Unter der immunsuppressiven Kortisontherapie nach der Pankreas-Transplantation kam es zu ansteigenden BZ-Werten am Tag, aufgrund von Stimulierung der Gluconeogenese in der Leber und im Folgenden zu nächtlichen Hypoglykämien durch ein aufgebrauchtes Glukosedepot der Leber.
-
Die sich im Verlauf entwickelnde Niereninsuffizienz erforderte eine langsame Reduktion der Insulindosis bei der Patientin, aufgrund des verminderten Abbaus des Insulins, welcher zu etwa 1/3 renal stattfindet.
-
Neben der erwähnten «Badewannenkurve» gibt es verschiedene andere, den Diabetologen gut bekannte BZ-Tagesprofilkurven, wie z. B. die Berg-, Tal-, Hügel-, Himmels- oder erratische (unvorhersagbare) BZ-Kurve. In Abbildung 3 und Tabelle 1 werden die Ausprägung und die Ursachen dieser Tagesprofile theoretisch zusammengefasst. Die Patientin durchlief im Verlauf ihrer Krankheit jede dieser charakteristischen Kurvenverläufe wiederholt.
Insgesamt erfordert die Langzeitbetreuung von Patientinnen und Patienten mit Diabetes Typ 1 ein grosses Mass an Erfahrung und bedarf interdisziplinärer Zusammenarbeit. Patientinnen und Patienten mit Typ 1 Diabetes erleben immer wieder neue Situationen, auf die flexibel und differenziert reagiert werden muss. Neben dem weithin bekannten, sich kaum ändernden Fachwissen (z.B. die erwähnten Gründe, die zu den typischen BZ-Tagesprofilkurven führen, welche häufig von erfahreneren Diabetologen übermittelt werden, jedoch häufig nicht in Lehrbüchern zu finden sind) sollten den Patientinnen und Patienten auch immer wieder die neuesten technischen Hilfen angeboten werden.
Die dargestellte Fallpräsentation zeigte einen extremen Verlauf des Typ 1 Diabetes, anhand dessen viele Situationen geschildert werden konnten mit denen Diabetologinnen und Diabetologen regelmässig konfrontiert werden. Wenn die Patientinnen und Patienten schon zu Beginn der Diagnose Diabetes mellitus Typ 1 eine adäquate Schulung erhalten, haben diese Patientinnen und Patienten heute sehr oft eine gute Chance, mit der Krankheit im Alltag angemessen umzugehen. Dadurch kann die Lebensqualität dieser Patientinnen und Patienten erhalten werden und eine Verkürzung der Lebensspanne deutlich verringert werden.20 Insgesamt bleiben derart dramatische Verläufe, mit fast allen denkbaren Komplikationen wie im vorliegenden Fall, eine Ausnahme.
Die Patientin zeigte ein beeindruckendes Durchhaltevermögen, sie gab nie auf und ist weiterhin bestrebt Ihren «Brittle Diabetes» in den Griff zu bekommen.
Fazit
Typ I Diabetes Patientinnen und Patienten erleben verschiedenste Blutzucker (BZ)-profile im Laufe Ihrer Krankheit. Deren Ursachen sind oft mehrdeutig und vielfältig und unter anderem abhängig von Essverhalten, Bewegung, unkorrekter Handhabung der Technik, Begleiterscheinungen der Insulintherapie oder anderen Therapien, Komorbiditäten und Stress. Manchmal sind BZ-Profile aber auch sehr suggestiv, wie die absichtlich in Kauf genommenen, hohen BZ-Werte nachts aus Angst vor Hypoglykämien, die zu einer Badewannenkurve (hoher Blutzucker morgens und zur «Bedtime», aber normal tagsüber) führen. Die Beurteilung der Blutzuckerprofile sind zentral in der Schulung und Betreuung der Patientinnen und Patienten mit Typ I Diabetes. Der Fall zeigt, dass auch erfahrenen Diabetologinnen und Diabetologen die bisherigen Werkzeuge der Insulintherapie nicht reichen, um solche BZ-Tagesprofile zu vermeiden. Es ist aber zu hoffen, dass die geplanten «semi-closed-loop» Insulintherapie bei der Patientin eine signifikante Verbesserung der BZ-Werte ermöglicht.
Conflicts of Interest
The authors declare that there are no commercial or financial relationships that could be construed as potential conflicts of interest.
Author Contributions
All authors contributed equally to this manuscript.
Funding
This work received no specific grant from any funding agency in the public, commercial, or non-profit sectors.
Acknowledgments
Writing and editing assistance was provided by H+O communications Ltd., Zurich, Switzerland.
-verlauf__differentialdiagnose__hoher_bz_morgens_bei_normal_.png)


-verlauf__differentialdiagnose__hoher_bz_morgens_bei_normal_.png)
